Se han retirado del mercado lotes del medicamento Remdesivir para el tratamiento del COVID-19 después de que se encontraran partículas de vidrio en algunos viales
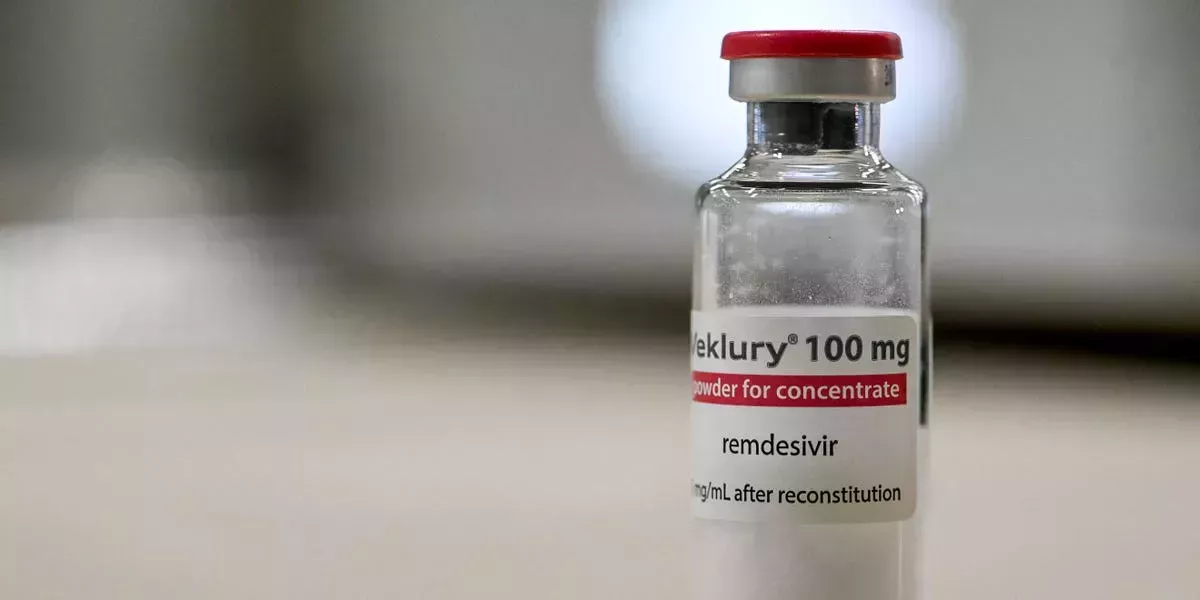
Se han retirado dos lotes del medicamento antiviral Remdesivir de COVID-19 después de que se encontraran partículas de vidrio en algunos viales.
Según un comunicado de Gilead Sciences, se está llevando a cabo la retirada de dos lotes del medicamento en todo el país.
"Gilead Sciences Inc. recibió una queja de un cliente, confirmada por la investigación de la empresa, sobre la presencia de partículas de vidrio", dijo Gilead en un comunicado.
¿Qué hacer para la caída del cabello después del Covid? ¿Qué es bueno para la caída del cabello después del Covid?
"Un producto inyectable que contenga partículas de vidrio puede provocar una irritación o inflamación local en respuesta al material extraño", añadió la empresa. "Si la partícula de vidrio llega a los vasos sanguíneos, puede desplazarse a varios órganos y bloquear los vasos sanguíneos del corazón, los pulmones o el cerebro, lo que puede causar un accidente cerebrovascular e incluso provocar la muerte".
Los dos lotes, 2141001-1A y 2141002-1A, se distribuyeron a los mayoristas entre el 25 de octubre y el 2 de noviembre. El portavoz de Gilead, Chris Ridley, declaró a Bloomberg News que esta retirada afecta a unos 55.000 viales del medicamento, lo que equivale a dosis para unos 11.000 pacientes.
Sin embargo, Gilead señaló que no se habían notificado reacciones adversas en relación con los lotes retirados.
Remdesivir, que también se conoce como Veklury, es una de las terapias autorizadas por la FDA actualmente disponibles para los pacientes de COVID-19 y se administra por vía intravenosa durante diez días. El fármaco se utiliza en Estados Unidos desde mayo de 2020, cuando la FDA lo autorizó para uso de emergencia.
Remdesivir fue administrado al ex presidente Donald Trump cuando contrajo COVID-19 en octubre de 2020, y también recibió la aprobación total de la FDA ese mismo mes.
No está claro cuántos informes recibió Gilead sobre las partículas de vidrio. Gilead no respondió inmediatamente a una solicitud de comentarios de Insider.





_12.07.28.png)
